Исследования
Программа исследований по изучению фармакокинетики, противовирусной активности, безопасности, влияния пищи, лекарственных взаимодействий, проведенных в России и Тайланде, с участием здоровых добровольцев, пациентов с ВИЧ-инфекцией, с использованием диапазона доз препарата от 10 до 80 мг и плацебо-контролем
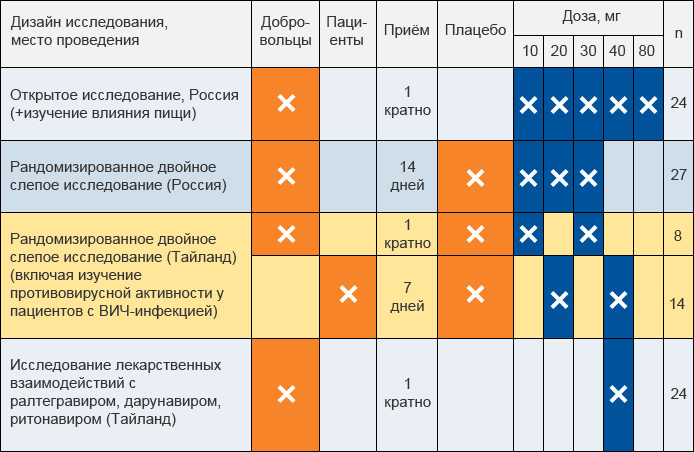
- Дозирование элсульфавирина 1 раз в день
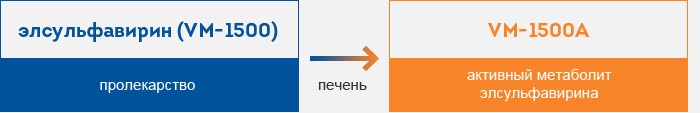
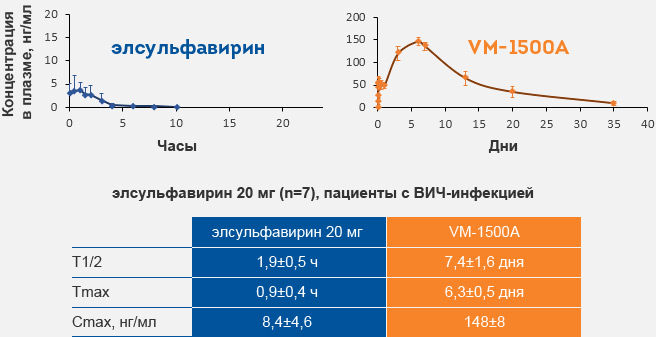
- Быстрое исчезновение элсульфавирина из плазмы, с образованием активного метаболита VM-1500A
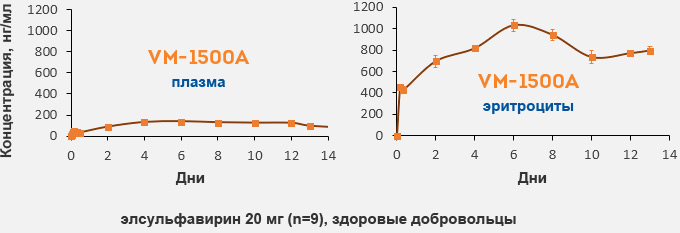
- Обратимое накопление VM-1500A в эритроцитах с последующим медленным высвобождением в плазму
- Обратимое связывание с карбоангидразой эритроцитов (продемонстрировано in vitro на клеточных экстрактах эритроцитов человека), без влияния на показатели газового обмена и кислотно-щелочного состояния
- Длительный период полувыведения VM-1500А из организма - 7-9 дней
- Наиболее длительный из применяемых третьих препаратов
- Меньшая «чувствительность» к пропуску дозы в отношения развития резистентности (особенно с учетом высокого генетического барьера резистентности)
- Возможность создания длительно действующих инъекционных форм (Long-Acting Injectable - LAI) на основе VM-1500A с режимом введения 1 раз в месяц и реже для поддерживающей терапии (см. раздел «Перспективы»)
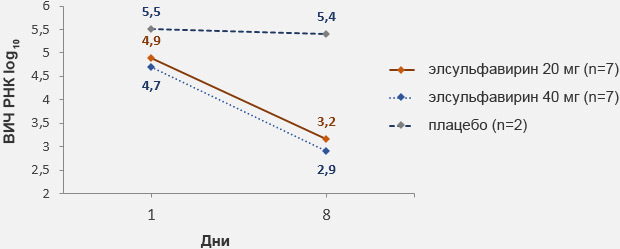
- Кравченко А.В., Орлова-Морозова Е.А., Шимонова Т.Е. с соавт. Эффективность и безопасность нового российского ненуклеозидного ингибитора обратной транскриптазы элсульфавирина в сочетании с тенофовиром/эмтрицитабином – многоцентровое сравнительное исследование с эфавирензом у пациентов с ВИЧ-инфекцией, ранее не получавших лечение. Инфекционные болезни, 2017, 15 (3): 5–13.
- Кравченко А.В., Орлова-Морозова Е.А., Шимонова Т.Е. с соавт. Эффективность и безопасность нового российского ненуклеозидного ингибитора обратной транскриптазы элсульфавирина в первой линии лечения ВИЧ-инфекции в комбинации с двумя нуклеозидными/нуклеотидными ингибиторами обратной транскриптазы – исследование 96 недель. Журнал инфектологии, 2018, 10 (2): 76-82.
- Этап выбора оптимальной дозы элсульфавирина: пациенты рандомизированно получали элсульфавирин 20 мг, элсульфавирин 40 мг (дозы препаратов были заслеплены) и эфавиренз 600 мг (по 30 пациентов в каждой группе).
- Выбрана оптимальная доза 20 мг на основании эффективности (равной во всех 3 группах) и переносимости (лучшей для дозы элсульфавирина 20 мг по сравнению с дозой 40 мг).
- Пациенты из группы 40 мг продолжили прием элсульфавирина в дозе 20 мг (далее «группа 40/20 мг», не вошла в анализ эффективности 48 недель, вошла в анализ эффективности 96 недель).
- Прямое сравнительное исследование элсульфавирина (в выбранной дозе 20 мг) с эфавирензом в дозе 600 мг в течение 48 недель в комбинации с тенофовиром/эмтрицитабином в качестве базовой терапии (по 60 пациентов в каждой группе, в обе группы дополнительно рандомизировано по 30 новых пациентов).
- Открытое наблюдательное несравнительное исследование в течение дополнительных 48 недель (до общей длительности лечения элсульфавирином 96 недель в выбранной дозе 20 мг) в комбинации с 2 препаратами из группы НИОТ, назначаемыми в соответствии с принятой клинической практикой.
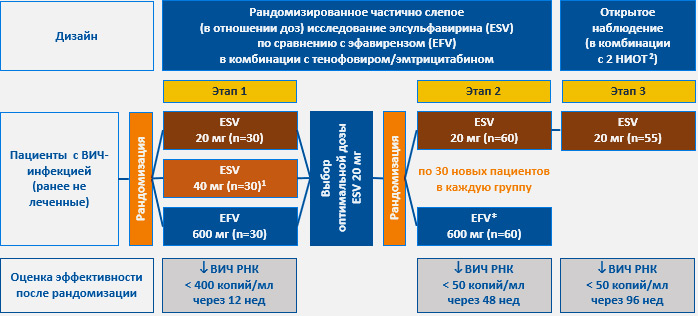
1 Пациенты группы «40/20 мг»:
— после этапа 1 переведены с дозы 40 мг на дозу 20 мг
— не включены в анализ 48 недель
— включены в анализ 96 недель: на 3 этапе все пациенты группы получали ESV 20 мг (n=26)
2 Комбинация 2 нуклеозидных/нуклеотидных ингибиторов обратной транcкриптазы (НИОТ) в соответствии с клинической практикой (доля пациентов, %):
— тенофовир/эмтрицитабин (35%), абакавир + ламивудин (21%), тенофовир + ламивудин
(19%), зидовудин + ламивудин (25%)
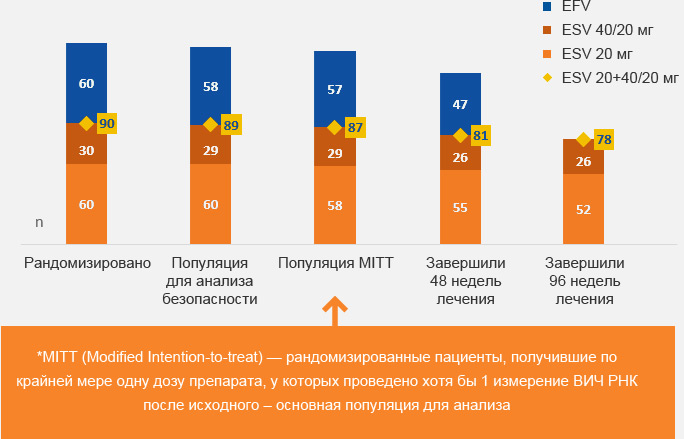
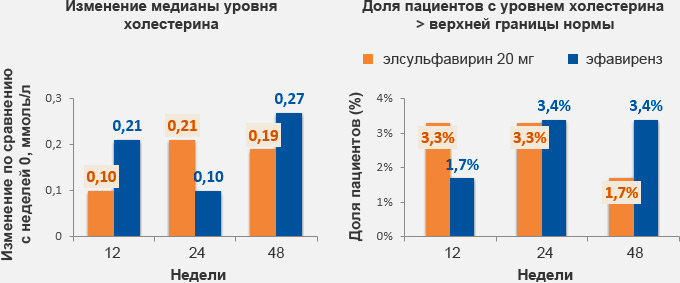
Отсутствие случаев развития резистентности
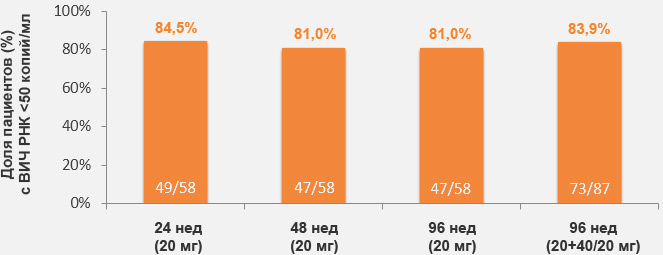
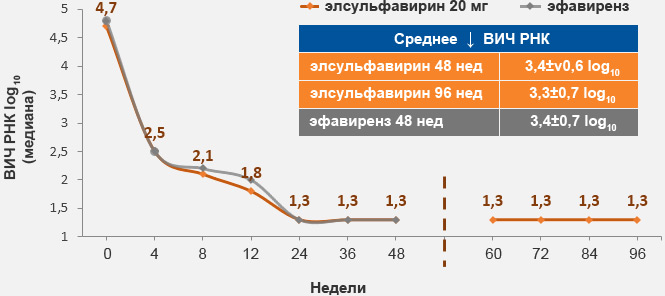
Более высокая вирусологическая эффективность элсульфавирина по сравнению с эфавирензом (на 24 неделе)
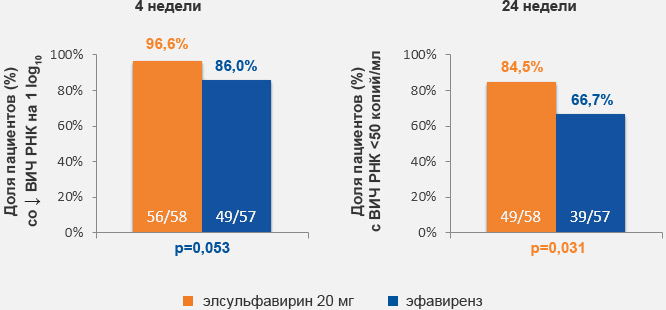
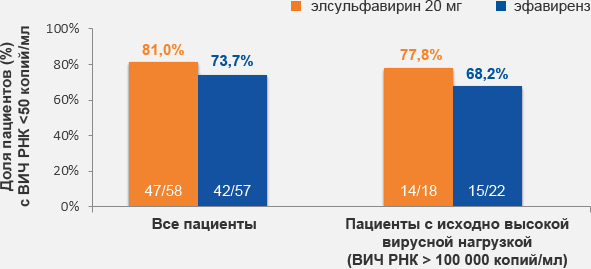
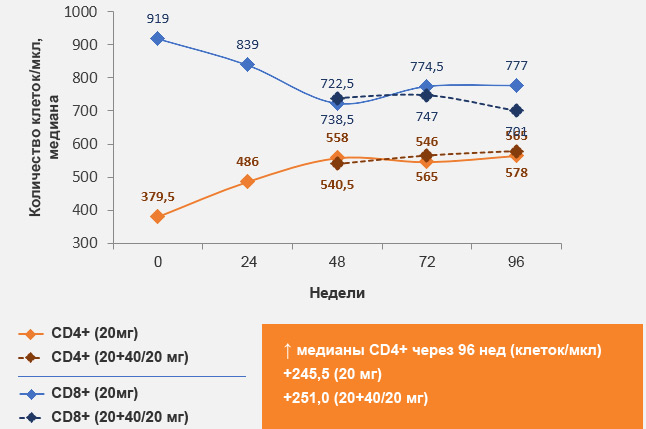
при применении элсульфавирина по сравнению с эфавирензом
(48 недель)
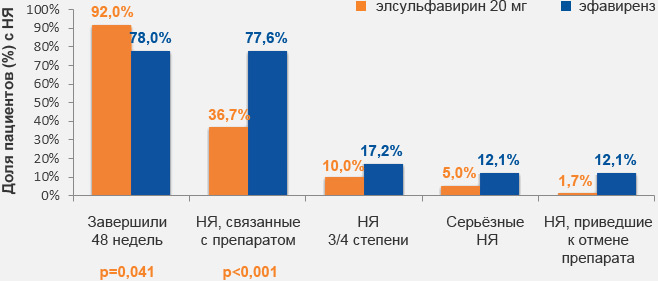
при применении элсульфавирина по сравнению с эфавирензом
(48 недель)
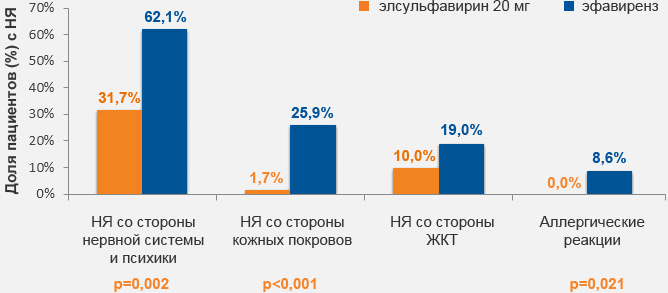
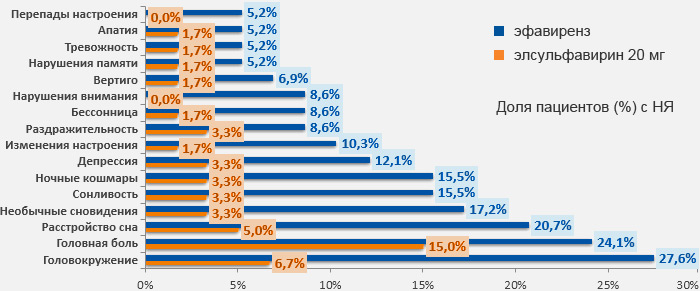
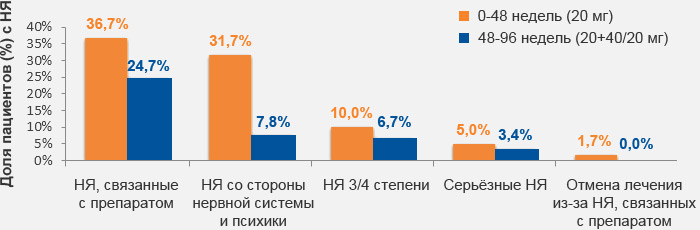

Национальные рекомендации по диспансерному наблюдению и лечению больных ВИЧ-инфекцией. Клинический протокол. 2017. Эпидемиология и инфекционные болезни. Актуальные вопросы, 2017, №6 (приложение), 80 с.
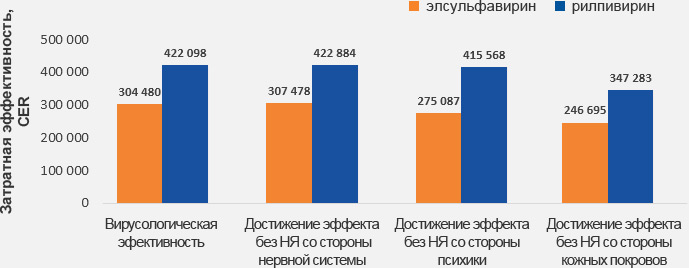
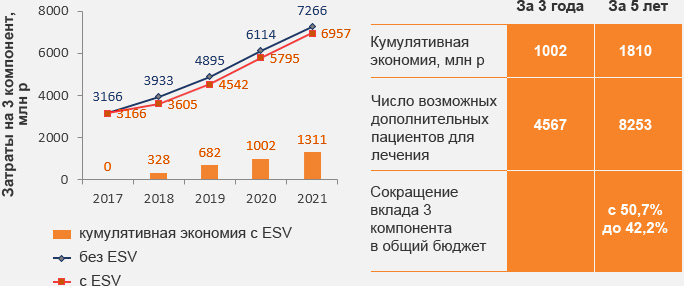
Экономия бюджета при применении элсульфавирина в 1-й линии лечения в рамках Программы государственных гарантий бюджета (федерального финансирования):
- сокращение расходов уже в 1-й год лечения
- кумулятивная экономия бюджета через 3 и 5 лет
- сокращение вклада 3-го компонента в общий бюджет лечения
В экспериментах in vitro были отобраны варианты ВИЧ-1, обладающие устойчивостью к активному метаболиту элсульфавирина VM-1500A в различной степени. Анализ мутаций данных вариантов вируса показал, что устойчивость к препарату может возникнуть по одному из двух механизмов:
- появление мутации V106I/A совместно с мутацией F227C (уровень резистентности повышается благодаря дополнительным мутациям A98G, V108I, E138K, M230L and P236L);
- появление мутации V106I совместно с мутацией Y188L (уровень резистентности возможно повышается благодаря дополнительным мутациям L100I, E138K and Y181C).
Данные изменения были введены в геном ВИЧ-1 дикого типа (изогенный штамм HXB2D), после чего были изучены уровни резистентности вирусов к VМ-1500А и эффективность репликации.
Было показано, что для возникновения значительной резистентности нужны как минимум две мутации (аминокислотные замены), за исключением аминокислотной замены Y188L, однако для появления последней требуется возникновение двух нуклеотидных замен.
Таким образом, элсульфавирин обладает более высоким генетическим баръером резистентности.
Варианты вируса, несущие мутацию F227C или четыре любых мутации, обладали пониженной способностью к репликации по сравнению с вирусом дикого типа штамма HXB2D.
Эти данные позволяют заключить, что профиль резистентности препарата элсульфавирин/VМ1500А отличается от профиля резистентности других препаратов класса ННИОТ (отсутствие перекрестной резистентности с другими ННИОТ).
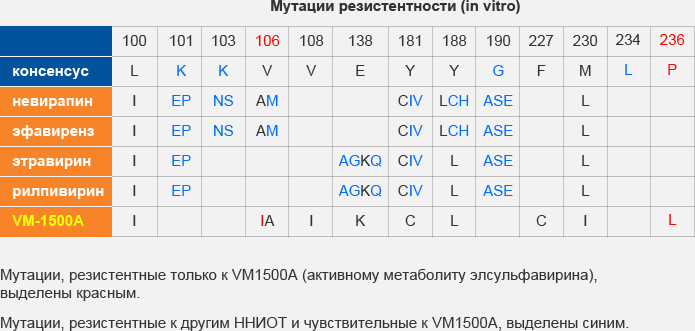
Мутации, резистентные только к VM1500A (активному метаболиту элсульфавирина), выделены красным.
Мутации, резистентные к другим ННИОТ и чувствительные к VM1500A, выделены синим.
В многоцентровом 96-недельном исследовании не выявлено случаев неэффективности терапии и развития резистентности к элсульфавирину.


